无掩膜直写光刻系统助力微流控芯片研发,实现肿瘤EV全面表征!
发布日期:2023-12-27

论文题目:An integrated sample-to-answer SERS platform for multiplex phenotyping of extracellular vesicles
发表期刊:Sensors and Actuators: B. Chemical IF: 8.4
DOI:https://doi.org/10.1016/j.snb.2023.134355
前言
肿瘤来源的细胞外囊泡(EV)正成为一种用于癌症诊断和肿瘤进展监测的非侵入性液体活检标志物。同时,EV多重表型分析有助于深入研究EV异质性、挖掘EV标志物,并促进其转化为常规临床应用。目前,临床缺乏可快速、灵敏、全面地分析EV蛋白质组学表型的检测技术。
近日,福建师范大学课题组提出了一种表面增强拉曼光谱(SERS)的微流控芯片,用于肿瘤来源EV的全面表征。该微流控芯片具有蛇形微结构,可实现样品的自动混合和处理,无需繁琐的人工操作流程。作者设计的多重SERS标记技术可同时表征EV表面的肿瘤相关生物标志物(PD-L1和EGFR),深入研究了不同肺癌细胞系EVs的特异肿瘤相关表型。该工作以An integrated sample-to-answer SERS platform for multiplex phenotyping of extracellular vesicles为题,在SCI期刊Sensors and Actuators B: Chemical上发表。
值得注意的是,本文中所制备的微流控芯片均使用小型台式无掩膜直写光刻系统- MicroWriter ML3制备。该设备全自动控制、结构小巧紧凑(70cm x 70cm x 70cm)、无需掩膜版、高直写速度及高分辨率等特点,为本实验提供了方便高效的微流控芯片加工方案。

小型台式无掩膜直写光刻系统- MicroWriter ML3
图文导读
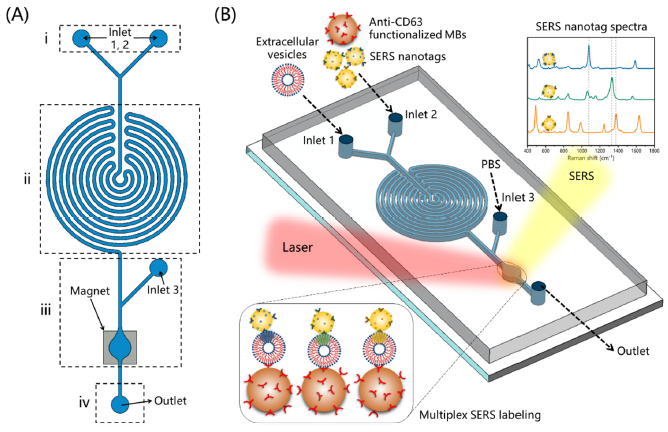
图1. (A)基于SERS的EV表型平台的结构和(B)工作原理图。(i)样品入口,(ii)蛇形微结构趋于用于混合和进行免疫反应,(iii)用于磁富集、洗涤和SERS检测的区域,以及(iv)样品出口。
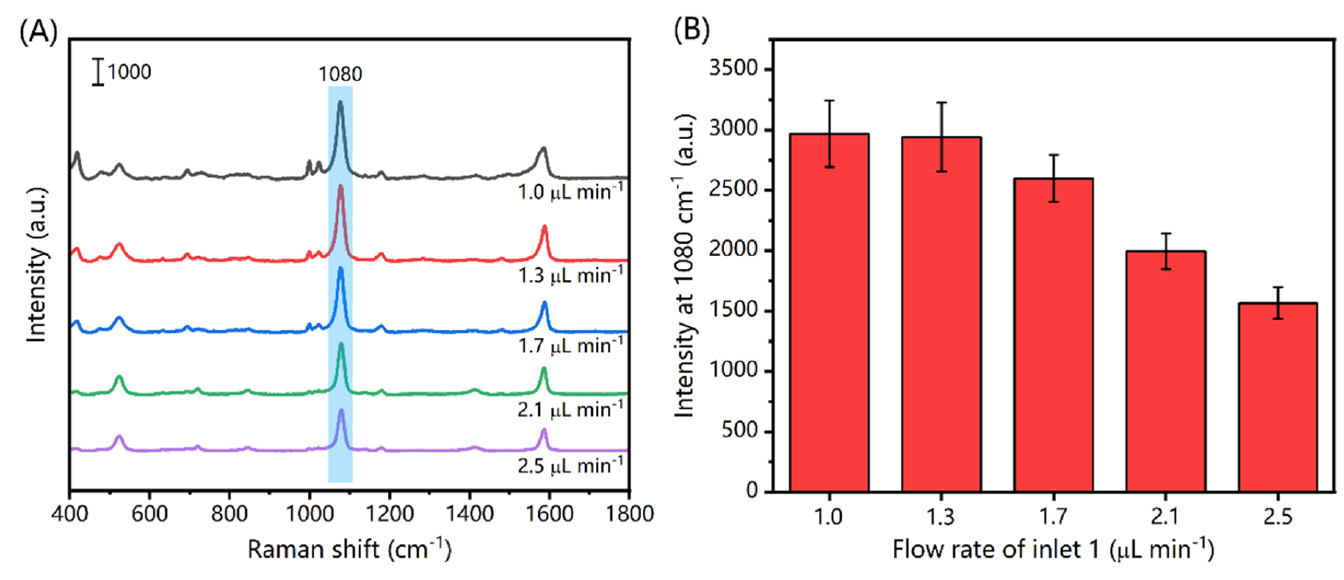
图2. (A)与流速相关的SERS光谱和(B)1080cm-1处的相应峰值强度值。
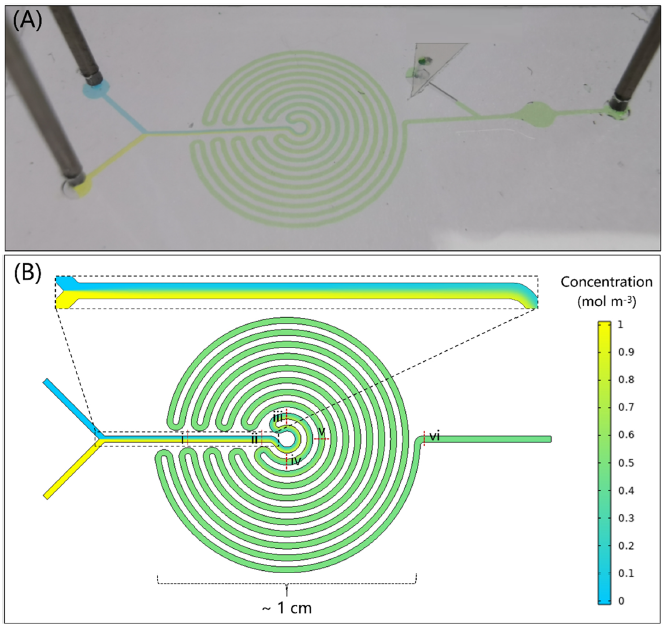
图3. SERS微流控芯片的混合能力表征。(A)蓝色和黄色液体分别从芯片的入口1和入口2注入芯片。(B)有限元模拟芯片不同区域液体的混合情况。

图4. 用NCI-H226所产生的EV来检测所制备的SERS微流控芯片的敏感度,EV的浓度为1.1 x 104 —1.1 x 1010 particles/ml。(A)在不同的EV浓度下CD63-MBA的纳米标签对应的拉曼图谱和(B)相应的线性回归拟合结果。(C)在不同的EV浓度下PD-L1-DTNB的纳米标签对应的拉曼图谱和(D)相应的线性回归拟合结果。(E)在不同的EV浓度下EGFR-TFMBA的纳米标签对应的拉曼图谱和(F)相应的线性回归拟合结果。

图5. 用所制备的SERS芯片表型多远EV。(A)不同肺癌细胞系的EV和肺支气管上表皮细胞系的EV进行SERS表征,(B)为相应的SERS特征值。三个细胞系的(C)PD-L1和(D)EGFR水平。(E)不同细胞系所产生的EV的SERS特征值。
结论
福建师范大学课题组利用小型台式无掩膜直写光刻系统- MicroWriter ML3制备了基于微流控芯片的SERS检测芯片。实验结果表明,芯片在定量检测肺癌细胞系来源的EV方面具有优异的灵敏度。此外,该芯片展示了其区分各种细胞系来源EVs的超卓能力,可提供EV生物学功能检测研究的新思路,并提供服务于临床癌症诊断和治疗监测的集成化技术。从文中可知,小型台式无掩膜直写光刻系统可以根据研究的实际需要,迅速地制备出相关微纳结构,保证了相关实验的顺利进行,为以微流控为手段检测和诊断癌症的研究提供可靠的技术保障。


