超精准可调节温度控制模块助力一篇Nat. Nano.!用于重复随机多路复用数据访问的热敏微胶囊中的 DNA 存储
发布日期:2023-08-07
本文转载自 宋杰课题组,作者孙鑫雨

背景:
由于其耐久性和高信息密度,DNA已成为归档数据存储的一种有吸引力的介质。可扩展的并行随机访问是任何存储系统所希望具备的理想特性。然而,对于基于DNA的存储系统,这仍需要得到稳健的确认。近期,Bas等[1]人报道了一种热限制PCR技术,它能够实现隔离的DNA文件的多路复用、重复的随机访问。该策略基于将生物素功能化寡核苷酸定位在热响应的半透性微胶囊内。在低温下,微胶囊对酶、引物和扩增产物是可渗透的,而在高温下,膜的坍塌防止了扩增期间分子间的干扰。该研究结果表明,与重复的随机访问相比,该平台优于非隔离的DNA存储,并且在多路PCR反应期间减少扩增偏差十倍。使用荧光分选,作者还演示了通过微胶囊条形码进行样品汇集和数据检索。因此,热响应微胶囊技术提供了一种可扩展的、序列无关的方法,用于重复的随机访问归档DNA文件。
实验结果:
作者设计的热限制PCR方法利用具有温度依赖性膜渗透性的微反应器来增强PCR扩增的准确性。使用这种策略,作者从复杂的DNA池实现多个DNA文件的多重,重复的PCR访问。作者的方法基于将生物素化的DNA文件稳定地封装在热响应的半透性微胶囊的个体群体内(图1a),然后对这些群体进行汇集。膜的独特热响应性渗透性极大地减少了PCR温度下的分子干扰和伴随的假象形成,从而允许多个数据编码的DNA文件被忠实地扩增。与乳化PCR相比,非生物素化的扩增产物可以在室温下从原始的数据编码的DNA文件中检索和分离,而不会破坏微隔室,因为膜渗透性在室温下得到恢复(图1b)。热限制PCR使用蛋白质组,即基于蛋白质-聚合物共轭物的半透性微隔室。生物素化的DNA文件可以通过封装的生物素结合蛋白Tamavidin 2-HOT稳定地定位在蛋白质组腔内。作者首先展示了在Tamavidin 2-HOT蛋白质组内生物素标记的DNA模板的热稳定保留。接下来,作者使用共聚焦荧光显微镜分析了蛋白质组对单链DNA(ssDNA)和双链DNA(dsDNA)的温度依赖性渗透性,并发现膜渗透性在较高温度下显著降低。基于这个观察结果,作者确定将个体反应隔离在蛋白质组内,在两个模板的多路复合PCR扩增期间显著降低了分子干扰。然后,作者将这些结果扩展到25个DNA文件的同时扩增,总共超过150万个独特序列。作者展示了与大规模扩增相比,当反应在蛋白质组内隔离时,多路复合扩增这个复杂DNA池会导致更均匀的序列表征。此外,作者证明蛋白质组可以通过共封装磁珠实现多次重复的读取操作,从而在PCR基础上实现随机访问后高效地恢复原始封装的DNA文件。最后,作者确认该平台与使用短DNA链和膜标签的荧光元数据标记兼容。此外,作者展示了结合荧光分选,可以根据元数据有选择地检索和扩增DNA文件,这是最近用于相似性和Boolean文件搜索的一种方法。
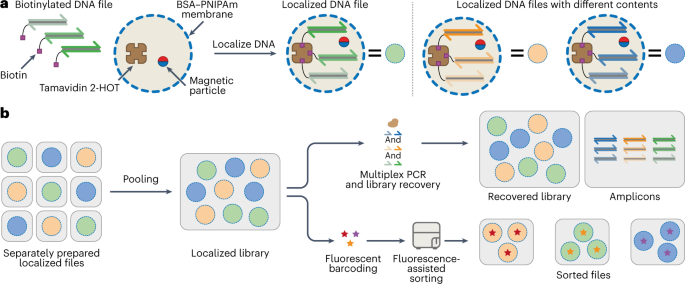
图1. 蛋白质组作为DNA信息存储的平台
为了了解蛋白质组的热性质如何影响封装的DNA文件的PCR,作者研究了蛋白质组的温度依赖性稳定性和渗透性。由于链霉亲和素仅在PCR期间使用的高温下部分耐受,因此作者使用热稳定的链霉亲和素类似物Tamavidin 2-HOT44,它与链霉亲和素的亲和力相似,但可以耐受PCR期间更高的温度。作者制备了含有4 µM链霉亲和素或4 µM Tamavidin 2-HOT的蛋白质组,以验证这两种蛋白在其中的热稳定性。然后,通过将双链DNA与蛋白质组一起孵育,将生物素化的、标记有Cy5的188 nt双链DNA A1F1定位在制备好的蛋白质组内。共聚焦显微镜图像显示,在加热至95°C后,只有使用Tamavidin 2-HOT制备的蛋白质组才能保留内部的双链DNA(图2a)。为了简化对蛋白质组的下游检索,作者还在蛋白质组内添加了超顺磁性颗粒。这两个改变共同产生了含有热稳定定位DNA和磁性检索的蛋白质组。当PNIPAm超过其临界溶液温度(LCST)时,它变得部分不相容,因此作者推断在LCST以上降低膜渗透性可以保留PCR处理过程中捕获的DNA分子(图2b)。为了研究ssDNA的温度依赖的渗透性,作者首先验证了在室温下封装Tamavidin 2-HOT的蛋白质组对ssDNA的渗透性。如预期的那样,ssDNA很容易穿过膜。因为ssDNA F2没有生物素化,所以洗涤捕获的蛋白质组会迅速失去荧光,表明在室温下,蛋白质组膜对ssDNA非常渗透(图2c)。接下来,作者制备了含有生物素化的21个核苷酸链A2和与之配对的Alexa-546标记的50个核苷酸ssDNA F2的10个核苷酸的段的Tamavidin 2-HOT蛋白质组,并将蛋白质组加热至95°C,以确保DNA双链完全熔化。在这个温度下的共聚焦成像实验显示,局部荧光随时间缓慢减少(图2d)。这个结果表明相对较长的ssDNA在这个温度下的膜渗透性要低得多。在95°C下使用长度为31个核苷酸的Alexa-546标记的ssDNA,DNA迅速渗透过膜。一旦冷却到LCST以下的温度,膜对长短ssDNA都再次高度渗透,表明温度诱导的膜渗透性变化是可逆的。综上所述,作者的结果显示,Tamavidin 2-HOT蛋白质组可以在高温下稳定定位生物素化的双链DNA,即使DNA双链熔化,膜的高渗透性也可以在冷却到LCST以下的温度时恢复。
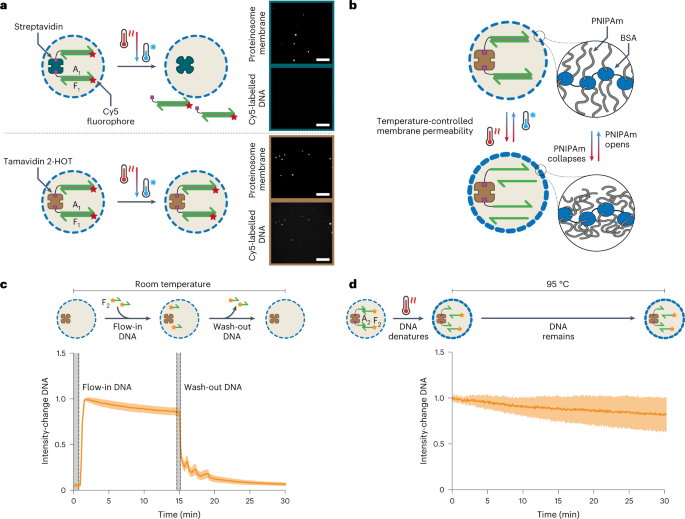
图2. 温度依赖性 DNA 定位
在确定生物素化的DNA在加热至PCR温度时仍定位于Tamavidin 2-HOT蛋白质组内,具有单个生物素修饰的长双链DNA的两个链即使双链DNA熔化时仍定位于蛋白质组内,膜渗透性可以通过温度控制后,作者进一步进行了蛋白质组内定位DNA模板的酶促扩增。为了展示含有内部Tamavidin 2-HOT的蛋白质组对DNA数据检索的通用适用性,作者接下来展示了定位的生物素化的DNA,其长度通常用于数据存储,可以使用PCR或SDA进行扩增(图3a)。为了在原位测量PCR下的局部dsDNA扩增,作者使用了定量PCR(qPCR; 方法)。含有4µM Tamavidin 2-HOT的蛋白质组被孵育于300 nM生物素化的178nt模板dsDNA T1A1或非生物素化的168nt对照dsDNA T1SU1。经过洗涤以去除游离模板后,作者添加了PCR反应混合物,包括聚合酶、脱氧核苷酸三磷酸(dNTPs)、引物和dsDNA敏感荧光染料EvaGreen。平均而言,当使用生物素化的dsDNA时,需要少4.4个循环才能达到荧光阈值,而非生物素化的dsDNA需要更多的循环(图3b)。假设在每个PCR循环中扩增完美,这表明与背景水平相比,生物素化的dsDNA可供扩增的dsDNA约为21倍,证明Tamavidin 2-HOT定位的dsDNA可供PCR扩增使用。接下来,作者使用SDA来等温扩增定位的dsDNA。含有T1A1的蛋白质组的SDA反应显示,平均扩增速率比孵育非生物素化的T1SU1的高8.6倍(图3c)。PCR和SDA的结果表明,Tamavidin 2-HOT定位的生物素化dsDNA,以及通常用于DNA数据存储的长度,可以从蛋白质组内部扩增。
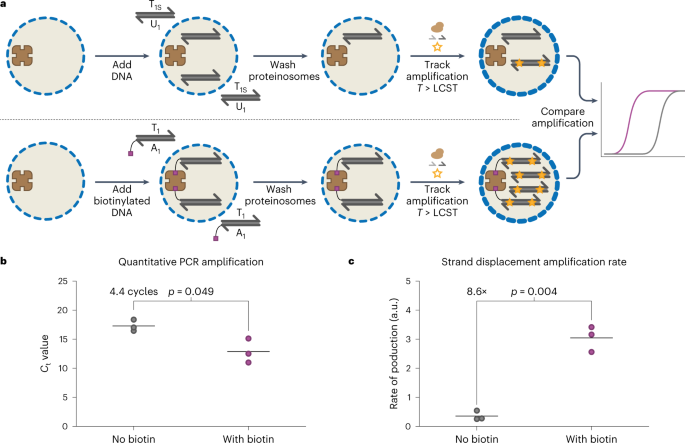
图3. 蛋白质组内定位的DNA的酶促扩增
基于PCR的随机访问可以从复杂的DNA池中检索编码数据。然而,包含高度相似的短区域的序列在PCR过程中容易发生重组。这种嵌合体的产生破坏了DNA文件,因为数据插入了错误的位置。此外,嵌合体的形成会导致复杂DNA池中的PCR偏差,以前采用乳化PCR来抑制此现象。作者认为,蛋白质组的温度控制的膜通透性应该在复杂DNA池的热限制性多重PCR中减少嵌合体的形成,因为在典型的PCR温度下,模板被有效地隔离(图4a)。为了研究热限制性多重PCR从定位的模板中如何影响嵌合体的形成,作者设计了两组生物素化的178nt长的dsDNA模板(T1A1和T2A3),它们共享一个31nt的互补区域,这样在多重PCR中形成的嵌合体C1C2长度为71bp(图4b)。为了将两个模板定位在分别含有4µM Tamavidin 2-HOT的单个蛋白质组中,作者采用了不同的生物素化策略来合成它们。T1A1被生物素化在其5'端,而T2A3被生物素化在其3'端。作者首先对单个蛋白质组进行了热限制性多重PCR,使用EvaGreen来检测扩增。作者发现,与未定位的模板相比,定位的模板产生更少的嵌合体,这表明蛋白质组的温度控制的膜通透性确实减少了嵌合体的形成(图4c)。作者还进行了混合DNA池的热限制性多重PCR,其中包含两个生物素化的模板和未标记的dsDNA,以模拟复杂DNA池。在使用定位的模板时,嵌合体的产生明显减少,这表明定位的模板在复杂DNA池中的热限制性多重PCR中仍然表现出较低的嵌合体形成率(图4d)。
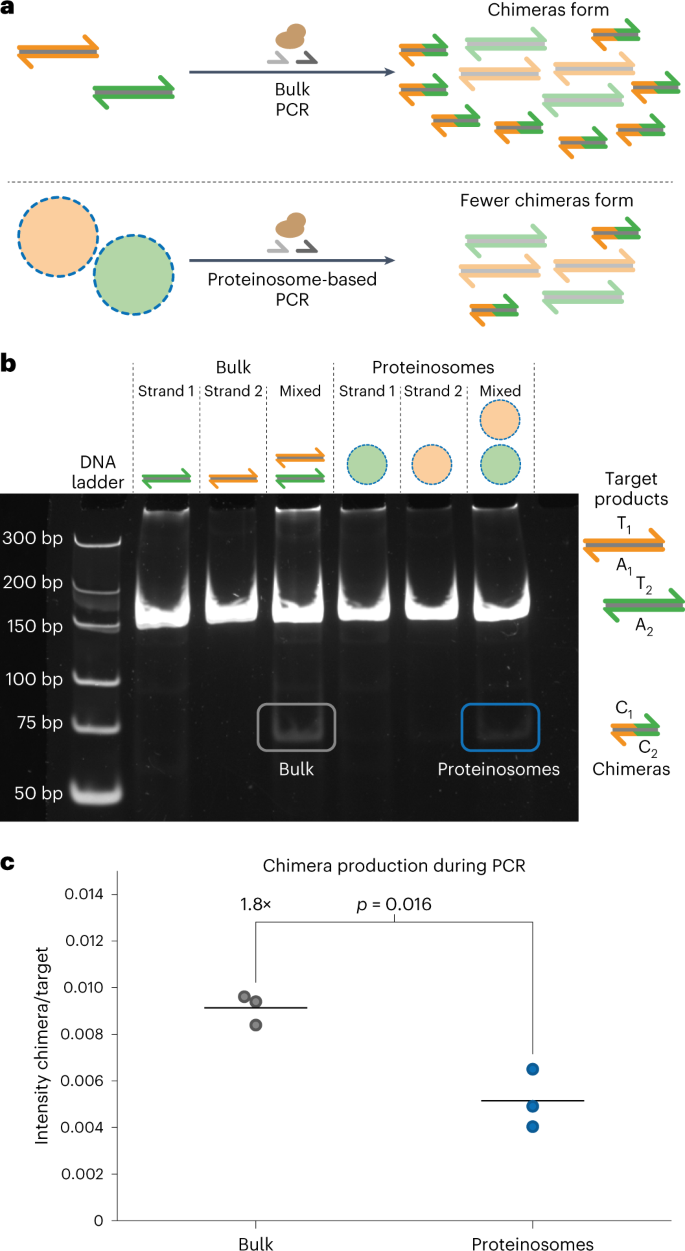
图4. 局部扩增可减少PCR过程中的分子串扰
由于生物素化的DNA仍然局限在Tamavidin 2-HOT蛋白质组内,作者预计在PCR后使用磁性分离来恢复蛋白质组和其封装的DNA编码文件,可以可靠地重复访问DNA编码数据。为了测试这一点,作者将三个文件定位在含有4 µM Tamavidin 2-HOT的蛋白质组内。在混合前,清洗了蛋白质组以创建基于蛋白质组的文库。此外,文件还以等摩尔浓度混合在批量中以生成非局限文库。从生成的文库中,文件在三个连续的批量、乳化或蛋白质组PCR回合中扩增,每个回合检索一个不同的文件。经过三轮后,作者再次访问了初始文件。重要的是,在PCR反应之间,作者使用磁性分离恢复了蛋白质组定位的文库,并重复使用该文库扩增下一个文件。使用批量PCR扩增的文库在使用之前通过灭活dNTP和引物进行纯化以用于扩增下一个文件。最后,通过破乳和自旋柱纯化对使用乳化PCR扩增的文库进行了纯化。使用Illumina测序,作者确定了文件内的丢失率(图5c)。作者观察到,重复访问基于蛋白质组的文库PCR产生了最低的序列丢失率,其次是乳化PCR和批量PCR(图5d)。这些结果共同表明,基于蛋白质组的DNA文件封装和随后的大规模DNA文库汇集,简化了可靠的重复多路PCR操作。
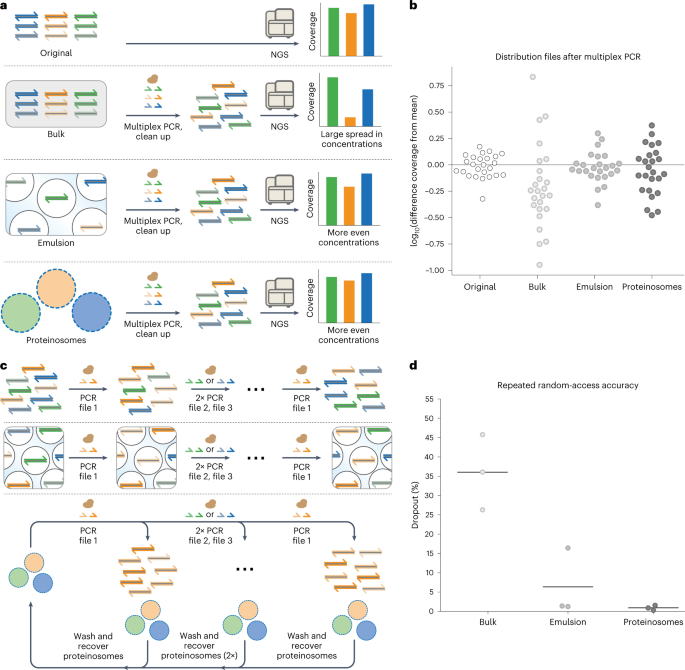
图5. 多重PCR和蛋白质组内DNA编码文件的重复访问
PCR基础的DNA文件检索非常特异性;然而,需要足够正交引物的需求限制了可以存储在单个池中的文件数量。这种限制导致了补充策略的开发,以实现随机访问DNA文件,例如物理分离、基于杂交的检索、另类扩增方案和基于荧光辅助的分选等。除了重复多路PCR外,作者还试图设计方法,以选择性地从DNA编码的蛋白质组文库中检索文件。为了实现这个目标,作者生成了一种基于荧光条形码蛋白质组群体的策略,该策略基于使用FITC和DyLight 405标记微囊膜,以及在初始数据编码DNA文件定位在蛋白质组内后添加短的生物素化的、Cy3(F4)标记或Cy5(F5)标记的单链DNA来进行条形码标记(图6a)。在将编码数据的DNA封装在带有条形码的蛋白质组中后,作者汇集了各自的群体,并使用荧光激活细胞分选(FACS)从池中选择特定的文件(图6b),通过三步选择程序。荧光数据中仅观察到单峰分布,从而表明各个群体均匀。将池分离成单个群体后,作者使用qPCR来确定每个文件在分离群体中的比例,以确认正确检索到了编码的DNA数据(图6d)。作者发现,目标文件占排序样品中所有DNA的平均75.0%(每个非目标文件平均为8.4%),从而证明了对其他文件的富集。这些结果表明,蛋白质组不仅与基于PCR的随机访问兼容,而且基于荧光的蛋白质组元数据检索也是可能的。对于基于DNA的数据存储,DNA的长期稳定性至关重要。先前的研究已经表明,DNA的冻干可以将DNA的水解稳定性提高约一个数量级。作者在海藻糖存在下对包含内部DNA的蛋白质组进行了冻干。显微镜和qPCR实验表明,在固体粉末重新溶解后,DNA的完整性和共定位在蛋白质组内没有受到影响。重要的是,在重新溶解后,作者没有观察到蛋白质组的聚合。
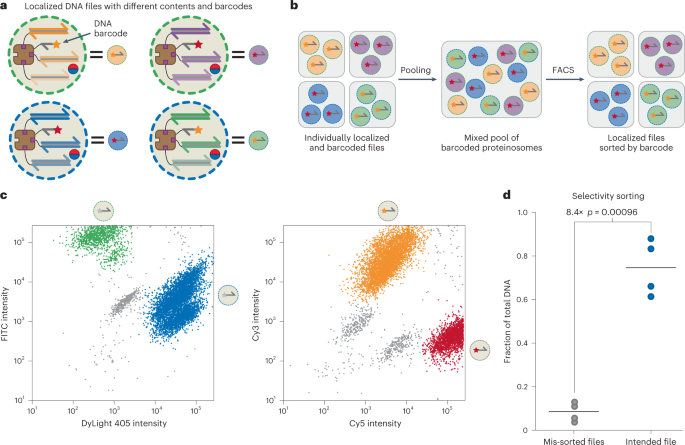
图6. 荧光辅助分选蛋白质组,用于选择性的文件检索
总结与讨论:
随着DNA合成和测序技术的进步,将数字数据长期存储在DNA上已成为可能。然而,迄今为止,反复和并行的基于PCR的随机访问仍然具有挑战性。本研究开发了一种基于热响应性半透膜微小隔室的方法,实现了与乳化PCR相当的多重PCR随机访问性能。然而,与乳化PCR不同的是,在扩增和数据检索后,封装的DNA编码文件仍然保持在微小隔室内,因此使得原始文件编码分子可以重复复制。此外,作者还加入了基于荧光的条形码,并将其用于基于微小隔室的文件排序,提供了额外的数据组织层次。在当前的DNA合成价格下,使用微小隔室进行DNA文件定位不会导致每MB存储数据的价格显著增加,而微小隔室定位的数据的物理密度与其他DNA封装方法相当。与乳化PCR相比,基于微小隔室平台的DNA编码数据文件的初始定位相对耗时;然而,一旦定位,封装的文件是完全可访问的,无需进行大量的处理步骤,简化了数据检索。未来的研究将致力于使用加速老化试验研究干燥状态下封装的DNA的长期稳定性。
超精准可调节温度控制模块VAHEAT介绍:
本文中,微胶囊的温度限制渗透性研究使用的是超精准可调节温度控制模块-VAHEAT,该模块在长时间(小时到天)和短时间(秒到分钟)下的温度稳定性可至0.01°C (RMS),加热速率可达100℃/s,温度可达200℃,不仅为该实验提供了快速和精确的温度控制,同时也保证了优越的成像质量。

超精准可调节温度控制模块-VAHEAT
VAHEAT主要特点:
☛ 温度稳定性高:0.01℃
☛ 温控范围广:RT-200℃
☛ 优越的成像质量
☛ 快速且可靠,用于油浸物镜
☛ 四种加热模式可根据用户需求进行不同的实验
VAHEAT典型案例:

VAHEAT部分客户:

VAHEAT部分发表文献:
1. An inkjet-printable fluorescent thermal sensor based on CdSe/ZnS quantum dots immobilised in a silicone matrix. Sensors and Actuators A, 2022.
2. Colloidal black gold with broadband absorption for photothermal conversion and plasmon-assisted crosslinking of thiolated diazonium compound. ChemRxiv, 2022.
3. Mechanistic Insights into the Phase Separation Behavior and Pathway-Directed Information Exchange in all-DNA Droplets. Angewandte Chemie, 2022.
4. Reversible speed control of one-stimulus-double-response, temperature-sensitive asymmetric hydrogel micromotors. Chemical Communications, 2022
5. Progress and Challenges in Archaeal Cell Biology. In: Ferreira-Cerca, S. (eds) Archaea. Methods in Molecular Biology, 2022.
6. Phase-separation antagonists potently inhibit transcription and broadly increase nucleosome density. Journal of Biological Chemistry, 2022
7. A DNA Segregation Module for Synthetic Cells. Small, 2022
8. Precision size and refractive index analysis of weakly scattering nanoparticles in polydispersions. Nature Methods, 2022
9. The Spo13/Meikin pathway confines the onset of gamete differentiation to meiosis II in yeast. EMBO Journal, 2022
10. Microscale Thermophoresis in Liquids Induced by Plasmonic Heating and Characterized by Phase and Fluorescence Microscopies. The Journal of Physical Chemistry C, 2022.
11. A synthetic tubular molecular transport system. Nature Communications, 2021.
12. Deprotection of centromeric cohesin at meiosis II requires APC/C activity but not kinetochore tension. EMBO Journal, 2021.
13. Are bacteria claustrophobic? The problem of micrometric spatial confinement for the culturing of microorganisms. RSC Advances, 2021.
联系我们:
为了更好的为国内科研工作者提供专业技术支持和服务,Quantum Design中国北京样机实验室引进了VAHEAT超精准可调节温度控制模块,为您提供样品测试、样机体验等机会,期待与您的合作! 欢迎您通过电话:010-85120277/78、邮箱:info@qd-china.com或扫码下方二维码联系我们。

若您对设备有任何问题,欢迎扫码咨询!
参考文献:
1. Bögels, B.W.A., et al., DNA storage in thermoresponsive microcapsules for repeated random multiplexed data access. Nature Nanotechnology, 2023.


