Bioactive Materials:血管生成的重大突破——基质硬度通过 p-PXN-Rac1-YAP 信号轴调节前沿细胞形成
发布日期:2021-08-23

【研究背景】
血管生成是指从现有血管中内皮细胞生长而生成新的血管,一旦血管开始生成,被称为前沿细胞的特殊内皮细胞就会开始发芽过程。由此,血管芽内皮前沿细胞的长出标志着血管生成的开始,这一过程在生理学和病理生理学过程中关重要。然而,细胞外基质(ECM)的机械特性如何调节前沿细胞的形成在一定程度上被忽视了。前沿细胞的特性是血管生成和组织工程的关键,它可以定向迁移到无血管区域,对终形成的血管形态起决定作用。迄今为止,各种生化信号分子因素如 MST1-FOXO1等多见报道,然而功能血管的建立需要生化和生物力学信号线索的结合,后者取决于组织工程和再生医学中使用的生物材料的特性。
近期,北京大学口腔医学院的郭亚茹博士以作者在Bioactive Materials发表了题为:Matrix stiffness modulates tip cell formation through the p-PXN-Rac1-YAP signaling axis的研究文章。文章报道了基质硬度通过p-PXN-Rac1-YAP信号轴调节前沿细胞形成,这项工作不仅有助于在组织工程和再生医学中寻找佳材料,也为肿瘤治疗和病理性血管再生提供了新的治疗策略。在生物材料设计和治疗一些病理情况方面具有特殊意义。邓旭亮教授为本文通讯作者。

【研究概述】
在这项研究中,作者研究了基质硬度对前沿细胞形成的影响,并探索了基础机制。在肝癌细胞的外层发现CD31表达更高,组织硬度也更高。基质的硬度增加可以显著增加血管的生成和前沿细胞富集基因的表达。硬度较大的基质增加了FAK和p-PXN的局灶黏附,提高了活性Rac1的水平,进而导致细胞骨架组织和细胞刚度增加。随后,YAP作为下游的力效应因子被激活并易位入核,上调靶基因的表达,终促进前沿细胞的形成。p-PXN还可以减少细胞间的连接,从而促进前沿细胞的形成。由此表明:基质硬度可通过p-PXN-Rac1-YAP信号轴调节前沿细胞的形成。
【研究结果】
硬度的增加还可以促进血管的生成(图1D),从三维(3D)EC球体(图1E)的芽入侵距离增加可证明这一点。与GM60和GM30凝胶(图1F)相比,硬凝胶(GM90)中球体的芽数量增加了2倍。qPCR分析表明,前沿细胞富集基因,包括CD34、VEGFR2、DLL4、CXCR4、EFNB2和IGF2,在GM90基质(图1G)中显著上升。同时,更硬的凝胶中芽的宽度更厚,矩阵中含有更多和长的纤维状体(图1H和I)。由此数据表明,基质硬度增加可以促进血管生成和前沿细胞的形成。
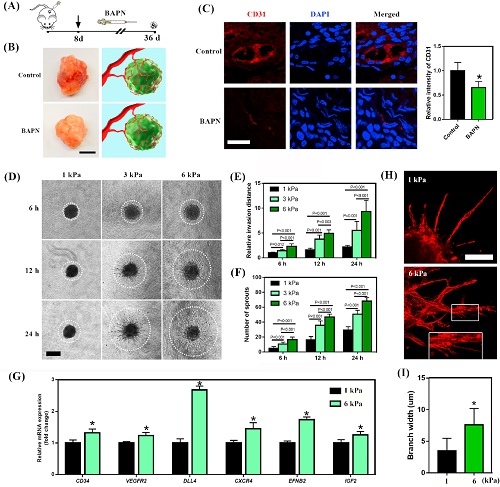
图1. 基质硬度增强血管生成和前沿细胞在体外和体内的形成。
在EC球形发芽模型中,从球体中产生的外层细胞和以下细胞分别被定义为前沿细胞和茎细胞。未爬出球体的细胞被定义为密集细胞(图2A)。通过原子力显微镜(AFM),我们检测到每个细胞的16个位置,并制作了典型的力学热图(图2B)。前沿细胞的刚度在数量上是茎细胞的两倍,是咽细胞的四倍(图2C)。此外,免疫荧光染色表明,前沿细胞显示长应力纤维的增强组装,而在茎和密集细胞作用捆绑是相对较短的,并限制在细胞外围(图2D)。研究人员发现前沿细胞中的YAT显示出明显的核定位,而YAT在咽细胞(图2D和E)中成为细胞质。通过免疫荧光、多功能单细胞显微操作系统FluidFM技术和原子力显微镜AFM,发现细胞扩散区域增加(图3A),粘附力(图3B和C)和细胞硬度(图3D),这表明 EC-ECM 连接增加,并通过 ECM 硬化提升细胞机械特性。另外,VP(YEP抑制剂)治疗显著降低了EC球体的延伸次数和芽入侵距离(图2F和G)。前沿细胞富集基因也被VP(图2H)抑制。因此,可以推断基质硬度调节了ECs的细胞机械感知和机械传输,促进了YAC活化,终增强了前沿细胞的形成。

图2. 前沿细胞、茎细胞和密集细胞的机械特性差异。
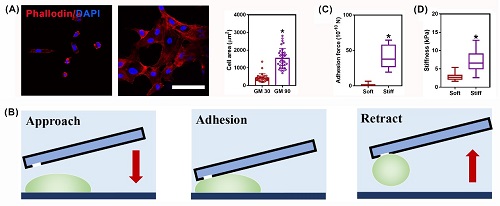
图3. FluidFM粘附力检测过程示意图。
在确定了血管生成和前沿细胞形成中EC亚型之间的机械差异后,作者探讨了ECM刚度通过PXN磷化调节前沿细胞的形成,验证了 p-PXN 在硬 ECM 诱导前沿细胞规范中的参与程度,进而推断,通过基质硬化强加的前沿细胞形成需要PXN磷酸化。随后,作者验证了p-PXN-Rac1-YAP激活在ECM僵硬诱导前沿细胞形成和血管生成体内的作用,研究人员通过在裸鼠体内皮下注射 HepG2 细胞创建肿瘤模型,并从第 8 天起每天使用 VP 治疗一次(图4F)。4周后,在肿瘤胶囊(图4G)上发现发芽较少的血管,CD31、CD34和VEGF强度(图4H,图4I )。VP治疗减少肿瘤体积(图4J)。这些数据表明p-PXN-Rac1-YAP信号轴与ECM硬化促进的前沿细胞形成和血管生成有很大关系。

图4. p-PXN-Rac1 通过激活 YAP 促进前沿细胞的形成和血管生成。
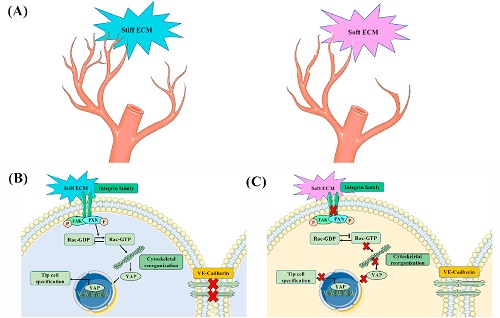
图5. 发芽血管生成受ECM硬度影响的潜在机制的示意图。
综上,基质的硬度增加可以显著增加血管的生长、发芽和前沿细胞富集基因的表达。硬度较大的基质增加了FAK和p-PXN在局灶黏附,提高了活性Rac1的水平,进而导致细胞骨架组织和细胞刚度增加。随后,YAP作为下游的力效应因子被激活并易位入核,上调靶基因的表达,终促进前沿细胞的形成。
【研究意义】
本研究加深了我们对前沿细胞形成和血管生成机理的理解,有助于优化组织工程和再生医学的生物材料设计,为一些病理情况提供新的治疗策略。无论是组织工程还是血管再生,都应考虑机械特性,如针对前沿细胞形成的刚度,以设计佳功能生物材料。此外,ECM可以在许多病理状态下变硬,如癌症的发展过程,随着变硬癌周围前沿细胞数量的增加,迫切需要靶向p-PXN、Rac1或YAP的药物来有效防止肿瘤的生长和转移。
【研究利器】——FluidFM技术在生物活性材料领域的创新应用
本实验研究人员采用了多功能单细胞显微操作系统——FluidFM技术,实现了单个细胞的分离,单个细胞粘附力的测量。瑞士Cytosurge公司多功能单细胞显微操作系统——FluidFM,是集原子力系统、微流控系统、细胞培养系统为一体的单细胞操作系统。主要功能包括单细胞注射、单细胞提取、单细胞分离、单细胞粘附力的测定、生物3D打印等。实验中FluidFM探针以3 μm/s靠近细胞,设定力为100 nN。当探针连接到到达设定点的细胞时,在探针中施加-650 mbar 的力,并保持5 s,以确保细胞被探针完全抓取。然后,在保持-650 mbar的压力,以1 μm/s的速度将探针抬高100 μm的高度,从而将细胞从基板上完全分离。FluidFM系统完全记录了每个单细胞的Z轴高度和力距离曲线,并分析其粘附强度。每个条件下少测量并获得20个力距离曲线。所有细胞粘附测量实验过程都是在 37 °C在5% CO2细胞培养环境下进行。

图6. FluidFM进行单细胞分离示意图。

图7. FluidFM进行单细胞力谱测定示意图。
【文末小视频】
本研究实际DEMO视频
【联系方式】
为了更好的服务客户,Quantum Design中国子公司也为大家提供样品测试、样机体验机会,还在等什么?赶快联系我们吧! 电话:010-85120277/78 邮箱:info@qd-china.com,期待与您的合作!
【参考文献】
[1] Y. Guo, F. Mei, Y. Huang, S. Ma, Y. Wei, X. Zhang, M. Xu, Y. He, B.C. Heng, L. Chen & X. Deng. Matrix stiffness modulates tip cell formation through the p-PXN-Rac1-YAP signaling axis. (2021) Bioactive Materials.


